La insuficiencia venosa crónica (IVC) es una condición que afecta a muchas personas, causando síntomas como edema, dolor y sensación de pesadez en las piernas. Incorporar ejercicios específicos en la rutina diaria puede ser una forma efectiva de mejorar la circulación y aliviar estos síntomas.
En este blog, exploraremos algunos ejercicios beneficiosos para la IVC y cómo pueden ayudar a mejorar la calidad de vida. Además, destacaremos la importancia de los productos de terapia compresiva de Urgo Medical, como UrgoK1 y UrgoK2, en el manejo de esta condición.
¿Qué es la insuficiencia venosa crónica?
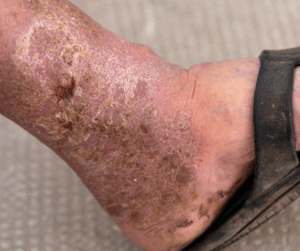
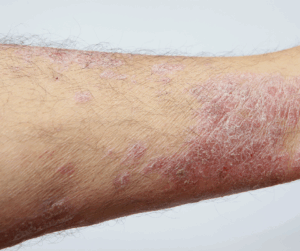
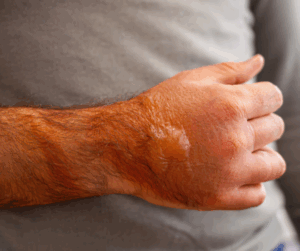
La insuficiencia venosa crónica (IVC) es una disfunción persistente del sistema venoso, caracterizada por reflujo, obstrucción o alteración de la bomba muscular, que conduce a hipertensión venosa, edema, cambios cutáneos y ulceración.

Ejercicios beneficiosos para la IVC
- Caminar: es uno de los ejercicios más simples y efectivos para mejorar la circulación en las piernas. Ayuda a activar la bomba muscular de la pantorrilla, facilitando el retorno venoso. Intenta caminar al menos 30 minutos al día.
- Elevación de piernas: Acuéstate sobre tu espalda y eleva las piernas por encima del nivel del corazón. Mantén esta posición durante unos minutos para reducir el edema y mejorar el flujo sanguíneo.
- Ejercicios de tobillo: Sentado o de pie, levanta los talones y luego los dedos de los pies, alternando entre ambos. Este ejercicio ayuda a activar los músculos de la pantorrilla y mejorar la circulación.
- Ciclismo: Ya sea en una bicicleta estática o al aire libre, el ciclismo es excelente para fortalecer las piernas y mejorar la circulación. Intenta pedalear durante al menos 20-30 minutos al día.
- Natación: es un ejercicio de bajo impacto que no solo mejora la circulación, sin que también es suave para las articulaciones. Nadar regularmente puede ser muy beneficioso para las personas con IVC.

Conclusión
Incorporar ejercicios específicos y utilizar productos de compresión adecuados son pasos esenciales para manejar la insuficiencia venosa crónica de manera efectiva.
En Urgo Medical, estamos comprometidos a proporcionar soluciones avanzadas que mejoren la calidad de vida de nuestros pacientes.