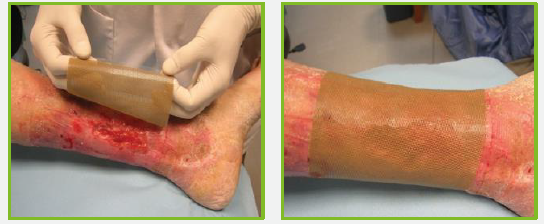
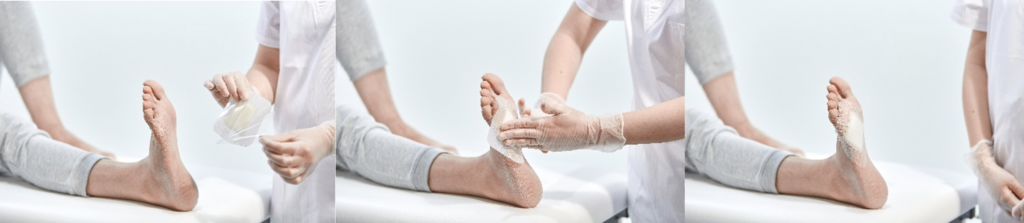
Algoplaque® es un apósito hidrocoloide estéril que se compone de:
- Una capa interna, compuesta por partículas hidrocoloides (CarboxiMetilCelulosa, CMC) insertas en una red de elastómero.
- Una capa externa compuesta por un soporte de poliuretano semipermeable, impermeable al agua y a las bacterias. También disponible en formato Sacrum.
MODO DE ESTERILIZACIÓN: Radio-esterilización.
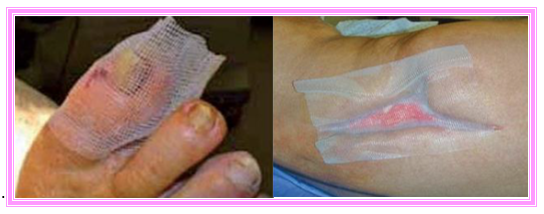
- En contacto con la herida, Algoplaque® / Algoplaque® Sacrum absorbe progresivamente el exudado y forma un gel húmedo que favorece el proceso de cicatrización regulando la humedad, la temperatura y el pH. El gel no-adherente evita daños en la herida cuando se retira el apósito.
- Algoplaque® / Algoplaque® Sacrum es transparente, lo que permite observar el gel y la evolución de la herida.
- Algoplaque® / Algoplaque® Sacrum es permeable al aire e impermeable al agua y a las bacterias. Estas propiedades permiten bañarse y ducharse, garantizan la protección de la herida frente a contaminantes exteriores, y permiten los intercambios gaseosos, que favorecen el drenaje de los exudados.
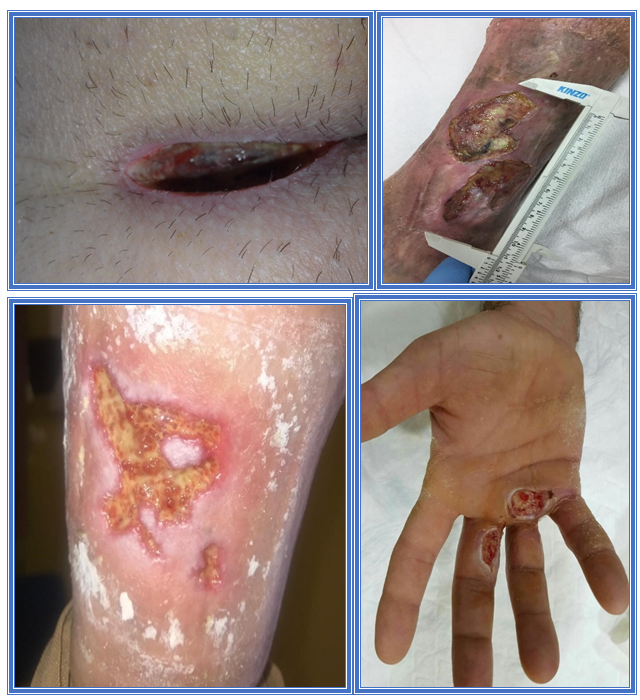
- Algoplaque® está indicado en el tratamiento local de úlceras de piernas y úlceras por presión con piel perilesional sana.
- Algoplaque® Sacrum está indicado en el tratamiento local de úlceras por presión con piel perilesional sana, especialmente en la zona sacral.
Contraindicaciones
- No usar en heridas infectadas.
- Preparación de la herida:
- Limpiar la herida con suero fisiológico. En caso de uso de antiséptico previo, aclare cuidadosamente la herida con suero
- fisiológico.
- Secar la piel perilesional con cuidado con una compresa estéril.
- Aplicación del apósito:
- Retirar las aletas de protección
- Aplicar Algoplaque® el apósito sin estirar sobre la herida. Asegurarse de no tocar la parte adhesiva del apósito con los dedos.
- Adherir suavemente el apósito en la herida y más firmemente hacia la piel perilesional.
- Aplicar Algoplaque® Sacrum adhiriendo suavemente el apósito en la herida y asegurándose que la parte angosta del apósito está dirigido hacia las nalgas.
- Por tener un border adhesivo, Algoplaque® Sacrum no necesita ser reforzado con un apósito secundario
- Cambio de apósito:
- En una herida limpia no infectada y cuando todos los tejidos necróticos hayan sido removidos, Algoplaque® se puede mantener durante varios días (3-4 días).
- En una herida al final de la etapa de desbridamiento y con restos de tejidos necróticos, Algoplaque® se tiene que cambiar más frecuentemente (cada 1 a 2 días)
- Si se observa filtración alrededor de los bordes en una herida muy exudativa, el apósito se tiene que cambiar de inmediato.
- Para un retiro indoloro, remover al apósito de forma tangencial, posicionando el apósito paralelo a la herida.
- Al retirar el apósito, el lecho de la herida puede verse cubierto de un film gelificado, que desaparecerá fácilmente aclarándolo.
- El uso de Algoplaque® en úlceras venosas no exime usar terapia compresiva si ha sido prescrito.
- El uso de Algoplaque® / Algoplaque® Sacrum en úlceras por presión no exime cuidados de enfermería apropiados.
- El protector estéril debe estar intacto antes de usar. No usar si el envase tiene daños*.
- Envase individual para apósito de uso único: reutilizar un apósito de uso único puede generar riesgo de infección.
- No esterilizar nuevamente.
- Almacenar puesto en forma horizontal
Tamaño | U / C | Referencia |
10 x 10 cm | 16 | 502881 |
15 x 15 cm | 10 | 505844 |
20 x 20 cm | 10 | 505843 |
Formatos financiados por la Seguridad Social
Tamaño | U / C | C.N. |
10 x 10 cm | 3 | 480269.6 |
15 x 15 cm | 3 | 480277.1 |