
UrgoStart Plus Border es un tratamiento que está compuesto por una matriz de la innovadora TLC-NOSF5, fibras de poliacrilato, capas superabsorbentes y un border adhesivo de silicona.
El apósito combina las siguientes 2 tecnologías:
- Fibras de poliacrilato de amonio que permiten un desbridamiento continuo a través de un desbridamiento electrostático 6.
- TLC-NOSF5 que permite acelerar la cicatrización al reducir el exceso de metaloproteinasas.
Eficacia:
- Limpieza continua y desbridamiento electrostático a través de las fibras de poliacrilato 6.
- Reducción del tiempo de cicatrización gracias a su matriz cicatrizante TLC NOSF.5
Funcionalidad:
- Mantenimiento de un ambiente húmedo favorable para la cicatrización
- Absorción vertical del exudado, limitando el riesgo de maceración.
- Borde adhesivo de silicona: sin memoria y reposicionable, impermeable y respetuoso con la piel perilesional.
La eficacia de la TLC-NOSF5 en la reducción del tiempo de cicatrización se ha demostrado en estudios clínicos controlados aleatorizados de doble ciego 2,3,4 y en un análisis de datos agrupados de 8 estudios observacionales, entre otros 5. Cuanto antes se inicie el tratamiento con TLC-NOSF5, más eficaz será 5.
La TLC-NOSF5 presente todos los apósitos UrgoStart contiene octosulfato de sacarosa, que permite reducir el exceso de metaloproteinasas que existe en las heridas de pacientes de edad avanzada y/o con patologías de base.
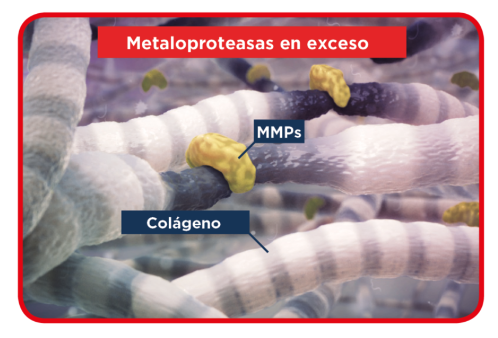
UrgoStart Plus Border se emplea en pacientes de edad avanzada y/o con patologías de base; la TLC-NOSF5 permite reducir el exceso de metaloproteinasas presente en estos pacientes para lograr reducir el tiempo de cicatrización.
UrgoStart Plus Border está indicado para toda herida superficial, no infectada, con o sin fibrina y esfacelo.
Contraindicaciones:
- UrgoStart Plus Border facilita el control de las pequeñas hemorragias de las heridas. Sin embargo, no debe utilizarse como una esponja quirúrgica para las heridas que sangran fuertemente.
- Para no retrasar ningún tratamiento óptimo, UrgoStart Plus Border está contraindicado en heridas cancerosas y heridas de fístula que pueden deberse a un absceso profundo.
- No utilizar cuando hay una sensibilidad conocida a UrgoStart Plus Border.
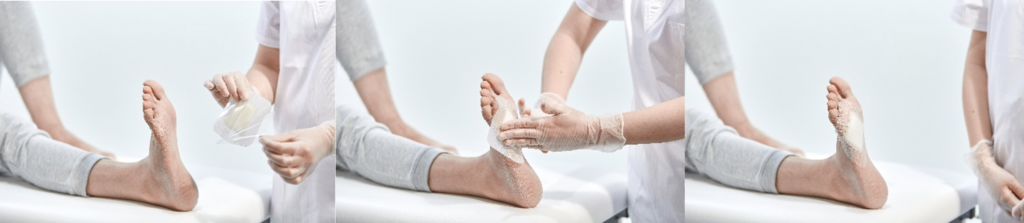
- Preparación de la herida:
- Limpiar la herida según el protocolo de cuidados habitual.
- Secar cuidadosamente la piel circundante
- El uso de UrgoStart Plus Border no dispensa la necesidad de desbridamiento mecánico si es necesario.
- Aplicación del apósito:
- Retire con cuidado las aletas de protección.
- Aplique el lado adherente de UrgoStart Plus Border sobre la herida.
- UrgoStart Plus Border no se puede recortar.
- Retirada del apósito:
- Presione sobre la piel sana, levante la esquina del apósito y retírelo con cuidado.
- Cambio del apósito:
- Según el nivel de exudado y el estado de la úlcera, UrgoStart Plus Border puede cambiarse cada 2 a 4 días y dejarse colocado hasta 7 días.
Precauciones:
- Al incluir una capa super-absorbente, la espuma central no debe ser recortada. Sin embargo, los bordes adhesivos pueden cortarse si es necesario usando tijeras estériles para adaptarse a diferentes formas de herida o cuerpo.
- Si la herida muestra signos de infección local, se recomienda que se use primero un tratamiento antimicrobiano como UrgoClean Ag antes de iniciar el tratamiento con UrgoStart Plus Border.
- En el inicio del tratamiento, la herida puede aparecer más grande debido a la eliminación gradual de tejido desvitalizado.
- En caso de uso de una crema, un ungüento, una emulsión, dejar secar la piel antes de la aplicación del apósito.
- UrgoStart Plus Border no debe ser utilizado en cámara hiperbárica.
- Apósito estéril, individual y de un solo uso: La reutilización de un apósito de un solo uso puede provocar riesgos de infección.
- No volver a esterilizar el apósito. Comprobar la integridad del protector de esterilidad antes de su uso. No utilizar si el envase está dañado.
Referencia | Código Nacional | Unidades / Caja | Medida apósito | Superficie activa | Recortable |
552576 | 188735.6 | 10 | 8×8 | 4,5×4,5 | No |
552577 | 188736.8 | 10 | 10×10 | 5,9×5,9 | No |
552578 | 188737.5 | 10 | 13×13 | 8,4×8,3 | No |
552675 | 188738.2 | 10 | 15×15 | 9,6×9,8 | No |
552297 | – | 5 | 20×20 | 14,3×12,6 | No |
Los productos UrgoStart vienen respaldados por multitud de estudios que sitúan esta gama con los máximos niveles de evidencia científica.
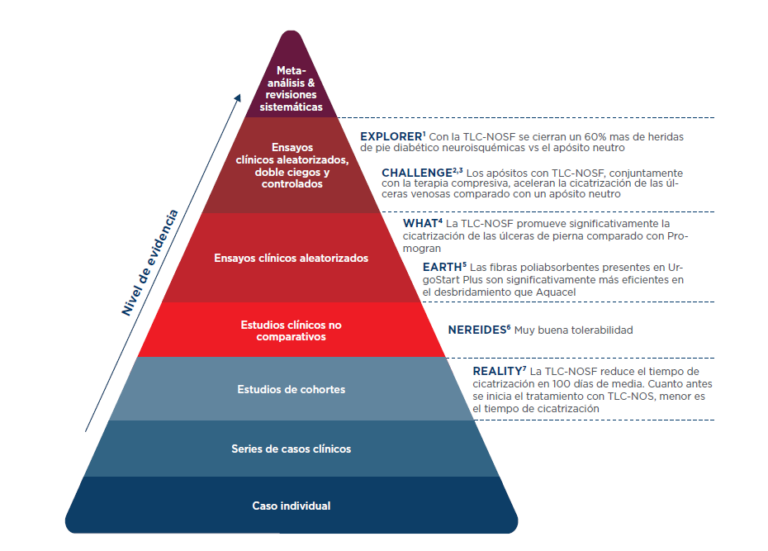
EXPLORER
Ensayo clínico multicéntrico internacional, doble ciego, randomizado y controlado, realizado en 240 pacientes (pie diabético neuroisquémico). Publicado en LANCET.
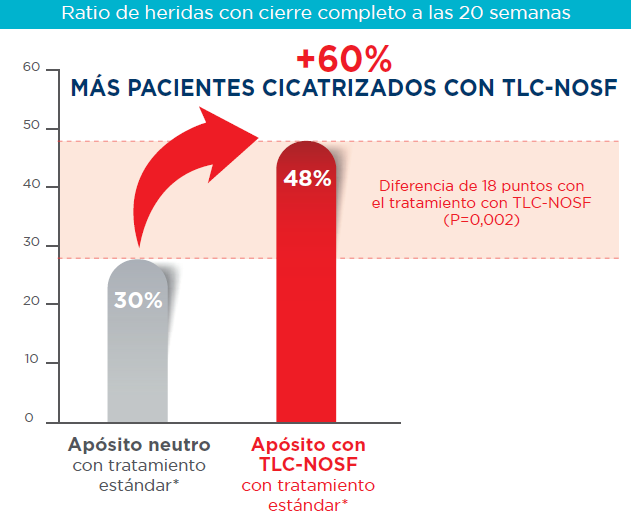
- Tasa de cierre completo de heridas en la semana 20: El uso de TLC-NOSF supuso un incremento estadísticamente significativo de la tasa de cierre completo en comparación con apósitos neutros, proporcionando el mismo nivel de cuidado (48 % frente a 30 %, p=0,002). Con los apósitos TLC-NOSF se obtuvo un 60 % más de heridas cicatrizadas que con los apósitos neutros.
- Tiempo para alcanzar el cierre completo de herida (en días): el uso de apósitos TLC-NOSF favoreció el cierre total de las heridas 60 días antes que con los apósitos neutros, proporcionando el mismo nivel de cuidados (p=0,029)
CHALLENGE
Ensayo clínico multicéntrico, doble ciego, randomizado y controlado, llevado a cabo en 187 pacientes (úlceras venosas y úlceras mixtas en la pierna)
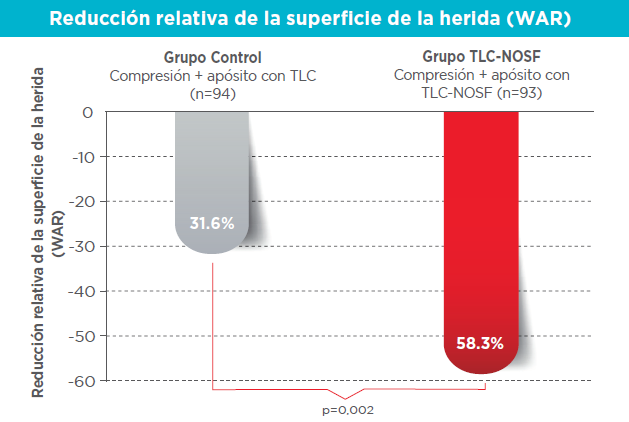
- Reducción relativa del área de la herida (WAR): superioridad estadísticamente significativa de TLC-NOSF tras un tratamiento de 8 semanas, donde se obtuvo una reducción del -58,3 % en las heridas tratadas con TLC-NOSF contra el -31,6 % en el grupo de control (p=0,002).
- También se observó una velocidad de cicatrización mucho mayor en mm²/día en el grupo TLC-NOSF en comparación con el grupo de control (10,83 mm²/día frente a 5,15 mm²/día; p=0,0056), lo que confirma un ritmo de cicatrización más rápido.
- Calidad de vida del paciente: Se ha demostrado que los apósitos TLC-NOSF mejoran sustancialmente la calidad de vida de los pacientes en comparación con los apósitos neutros. La reducción de la sensación de dolor y malestar (p=0,022), y de ansiedad y depresión (p=0,037) es también estadísticamente significativa
WHAT
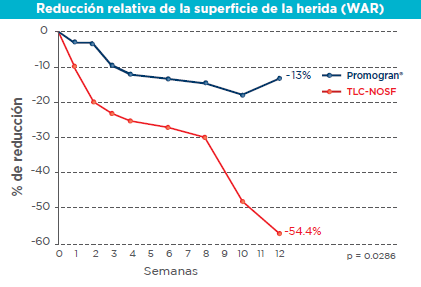
Ensayo clínico multicéntrico europeo, randomizado y controlado, realizado en 117 pacientes (úlceras venosas y úlceras de pierna mixtas):
- Reducción relativa del área de la herida (WAR): superioridad estadísticamente significativa de TLC-NOSF tras un tratamiento de 12 semanas, con el que se obtuvo una reducción del -54,4% en las heridas tratadas con TLC-NOSF frente al -12,9% en el grupo de control (p=0,0286).
- Tasa de cicatrización: significativamente superior en el grupo tratado con TLC-NOSF (p=0,029)
REALITY
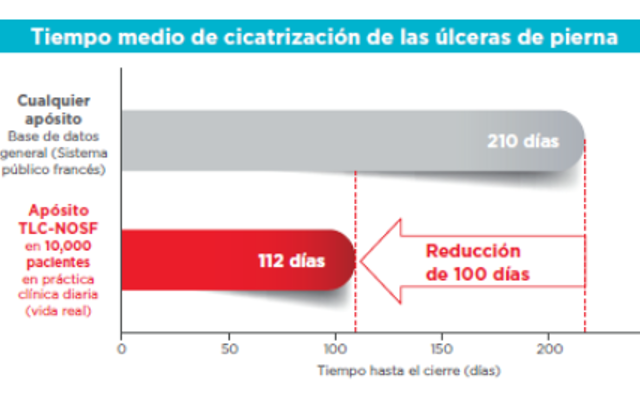
Análisis de datos agrupados de 8 estudios observacionales de casos reales, obtenidos de 10 220 pacientes (úlceras en la pierna, úlceras de pie diabético, úlceras de presión) 1
- Tiempo medio de curación: en promedio, el tiempo de curación con apósitos TLC-NOSF es de 111 días.
- El tiempo de cicatrización es menor si se comienza el tratamiento con TCL-NOSF desde la primera visita.
NICE
La guía Nice recomienda implementar UrgoStart en su práctica clínica para todos sus pacientes con úlceras de pierna, y úlceras de Pié Diabético para reducir el tiempo de cicatrización, mejorar su calidad de vida y ahorrar costes.

GUIAS DE REFERENCIA
Las nuevas guías del International Working Group of Diabetic Foot (IWGDF) consideran el uso de los apósitos TLC-NOSF en el tratamiento de las úlceras de pie diabético neuroisquémicas, no infectadas.

REFERENCIAS
- Informe del Ministerio de la Seguridad Social y del Parlamento sobre la evolución de las tarifas y productos de seguro médico en 2014. Julio de 2013.
- Edmonds M, Lázaro-Martínez JL, Alfayate-García JM, Martini J, Petit JM, Rayman G, Lobmann R, Uccioli L, Sauvadet A, Bohbot S, Kerihuel JC, Piaggesi A. Sucrose octasulfate dressing versus control dressing in patients with neuroischaemic diabetic foot ulcers (Explorer): an international, multicentre, double-blind, randomised, controlled trial. Lancet Diabetes Endocrinol. Marzo 2018; 6 (3): 186-196.
- Meaume S, Truchetet F, Cambazard F et al. A randomized, controlled, double-blind prospective trial with a Lipido-Colloid Technology-Nano-OligoSaccharide Factor wound dressing in the local management of venous leg ulcers. Wound Repair Regen. 2012; 20: 4, 500-511.
- Meaume S, Dompmartin A, Lazareth I, Sigal M, Truchetet F, Sauvadet A, Bohbot S. Quality of life in patients with leg ulcers: results from CHALLENGE, a double-blind randomized controlled trial. Journal of Wound Care. 2017; 26 (7): 368-379.
- Münter KC, Meaume S, Augustin M, Senet P, Kérihuel J.C. The reality of routine practice: a pooled data analysis on chronic wounds treated with TLC-NOSF wound dressings. J Wound Care. Febrero 2017; 26 (Sup. 2): S4-S15. Erratas: J Wound Care. Marzo 2017 2; 26 (3): 153.
